2020年,全球约有31.4万名女性被确诊患有卵巢癌,超过20.7万人死于该疾病。大约70%-80%的晚期卵巢癌患者在接受标准含铂化疗方案后仍会有疾病复发情况。这类患者目前仍存在未满足的临床治疗需求,亟需新的治疗方法。
1月3日,中国国家药监局药品审评中心(CDE)官网最新公示,第一三共(Daiichi Sankyo)递交的1类新药DS-6000a获批临床,拟开发治疗既往接受过至少一线全身抗癌治疗的铂耐药高级别卵巢癌、原发性腹膜癌或输卵管癌患者。公开资料显示,DS-6000a(raludotatug deruxtecan,R-DXd)一款靶向CDH6的抗体偶联药物(ADC)。2023年10月,默沙东(MSD)与第一三共达成一项高达220亿美元的合作共同开发后者的三个ADC,DS-6000a就是其中之一。
CDH6中文全称是钙粘蛋白-6或K-钙粘蛋白。研究显示,约65%~85%的卵巢癌肿瘤细胞中有CDH6表达,这与患者的疾病进展和生存率较低相关 。由于CDH6在肿瘤组织中高表达,而在正常组织中表达较少,并且抗体与其结合后ADC复合物能够迅速被内吞,因而CDH6被认为是治疗卵巢癌的潜力靶点之一。
DS-6000a是基于该公司的DXd ADC技术设计的一款潜在“first-in-class” CDH6靶向ADC。该候选药由人源化抗CDH6 IgG1单克隆抗体通过可裂解四肽连接子与多个拓扑异构酶I抑制剂有效载荷(一种依喜替康衍生物,DXd)连接组成。
在2023年欧洲肿瘤内科学会(ESMO23)年会上,研究人员曾公布了一项该药首次在人体中开展的开放标签、1期研究结果。22例病人,包括7例RCC和15例卵巢癌。研究数据显示,DS-6000a在既往接受过多种治疗且铂类耐药的晚期卵巢癌患者中持续显示出具有前景的临床疗效。患者的客观缓解率(ORR)为46%,同时观察到1例完全缓解(CR)、22例部分缓解(PR)和4例未经确认的缓解。患者的疾病控制率(DCR)达98%。中位缓解持续时间(DOR)为11.2个月。
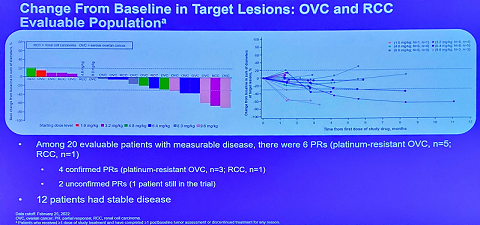
安全性方面,19 名患者出现了治疗引起的不良事件 (TEAE),最常见的 TEAE 是疲劳 (45.5%)、恶心 (45.5%) 和呕吐 (27.3%)。 4 名患者 (18.2%) 报告了 3 级或以上 TEAE,其中最常见的是中性粒细胞减少症 (13.6%)。 此外,1 例患者 (4.5%) 出现 3 级发热性中性粒细胞减少症,并发生 1 例 4 级血小板减少症 (9.6 mg/kg) 的剂量限制性毒性。
值得一提的是,第一三共在ADC药物开发中有明显技术领先优势。除了本次获批临床的DS-6000a,还包括:优赫得(靶向HER2的ADC)和datopotamab deruxtecan(Dato-DXd,靶向TROP2的ADC),这两款药正由第一三共与阿斯利康共同开发并在全球范围内商业化;patritumab deruxtecan,一款靶向HER3的ADC;ifinatamab deruxtecan,一款靶向B7-H3的ADC;以及DS-3939,一款靶向TA-MUC1的ADC。